|
癌症(Cancer)也叫恶性肿瘤(Malignant tumor),指的是细胞大量快速地非正常增生,且这些增生的细胞可能侵犯身体的其他部分。癌症是世界范围内主要致死疾病之一,目前已知的癌症超过一百种。& Z- A/ F) L6 ]& i9 S8 ]) q {6 d
z% s y7 _5 A4 k' m6 k
饿死肿瘤& N, L. q, l$ ^, R8 K$ A
0 i; A2 }, a9 T# q0 Z& C
1971年哈佛大学犹大·福克曼(Judah Folkman)教授在《新英格兰医学杂志》上发表文章说肿瘤的存在依靠血管新生(angiogenesis-dependent)。肿瘤的发育生长离不开血管的滋生,如果肿瘤自身的血液供给被切断,肿瘤将会停止生长、缩小或者死亡。这就是“饿死癌细胞”的最初设想,简单来说就是切断癌细胞的血液和营养供应。9 m2 N# Q! W7 `# a2 [, N
4 B" ~7 `1 D+ P L' ]- V; e8 I
德国的生物学家约翰内斯•科伊医生(Dr. Johannes F. Coy)也在《抗癌饮食》(The Anti-krebs Cookbook)一书中介绍,通过调整饮食,降低葡萄糖的摄入,长期依赖糖为营养的癌细胞,在持续的低糖饮食下会快速死亡。. v3 ~1 V& n6 E5 y/ v0 |, r
2 w* V: s( z' O2 K$ \- T. m! w
但是,癌症病人自身免疫力很低,再加上化疗的过程中会产生食欲低下的情况,营养跟不上,再不好好吃东西,淀粉和氨基酸等摄入不足,其结果是癌细胞没饿死,人先没了。所以,营养不良会降低肿瘤患者生活质量、缩短生存时间,营养治疗不足也是目前肿瘤患者5年生存率不高的重要原因之一。
, q/ [& j5 q" {$ [6 I1 _
$ `4 R+ J) P5 Y7 ? 上星期五11月8日《自然》的一篇文章表明,一种失败的抗癌药物的升级版不仅能够阻止肿瘤细胞摄取一种必需的营养物质-谷氨酰胺来饿死癌细胞,而且还能刺激免疫T细胞攻击肿瘤细胞的生长。
) Y2 |% g ^3 U0 q
; t; j) D: I6 x+ a; ^5 _6 O" A! B 该论文的文摘说:肿瘤的代谢特征为免疫细胞功能和癌症免疫疗法带来了重大障碍。使用一种新型的谷氨酰胺拮抗剂,在代谢上消除了肿瘤的免疫抑制性微环境。证明了在荷瘤小鼠中谷氨酰胺的阻滞抑制了癌细胞的氧化和糖酵解代谢,从而导致缺氧、酸中毒和营养耗竭减少。相反,T细胞明显上调氧化代谢并寿命更长、高度活化的表型来响应谷氨酰胺拮抗作用。细胞代谢和程序设计中的这些不同变化形成了有效的抗肿瘤反应的基础。因此,谷氨酰胺拮抗作用暴露了癌细胞和效应T细胞之间代谢可塑性的先前未定义的差异,该差异可被用作肿瘤免疫疗法的“代谢检查点”。" |8 a E! D& G! u/ d9 n4 b5 z
2 d1 y/ H! T6 T 文章说:癌细胞具有巨大的合成代谢和能量需求,并采用不同的代谢途径进行生长和存活。所谓瓦堡(Warburg)效应是指:癌细胞具有高度的糖酵解作用,它将葡萄糖代谢成乳酸。除了葡萄糖外,谷氨酰胺在提供合成代谢所需的碳和氮方面也起着重要作用。由于葡萄糖通过糖酵解途径代谢成乳酸,因此谷氨酰胺可以促进TCA循环,生成代谢中间体,以作为对合成代谢生长和增殖至关重要的脂质,蛋白质和核酸的基础。值得注意的是,这些相同的代谢程序也归因于促进与T细胞活化和增殖相关的巨大生长。癌细胞专门代谢的一个重要结果是,产生了一种低氧、酸性、营养贫乏的肿瘤微环境(TME),它对抗肿瘤免疫反应具有敌意。换句话说,癌细胞的专门代谢程序不仅可以促进肿瘤的生长,而且可以阻止有效抗肿瘤免疫反应的产生。
" d" O" x' [+ Q" M8 \! S" w& t" Q
x' \0 U9 u$ _9 G4 A 总结一下前面两段话:谷氨酰胺滋养了癌细胞,癌细胞的的代谢产生的微环境又遏制了免疫T细胞的生存。谷氨酰胺抑制剂即可饿死癌细胞,又可提高免疫力由T细胞杀死癌细胞。6 e, k& \2 B% V9 j6 ~% S# h9 F
$ s. {; o. }3 {# Z) X- ?5 ~谷氨酰胺与T细胞
6 O- Y4 w( s# N* v% k- t# \) r" {" t) N6 r
先来看看谷氨酰胺。1935年人们发现了哺乳动物体内的谷氨酰胺。1972年学者就发现“谷氨酰胺在恶性细胞氧化代谢中的作用”。
2 B, c) R8 I2 U; P1 v; {1 ~* ^" t
谷氨酰胺(Glutamine)为人体中含量最丰富的非必需氨基酸,人体可合成,储存在骨骼肌或血液中。在大运动量、受伤或患病时,需要补充谷氨酰胺或吃牛肉、牛奶(奶制品)、鸡肉、鸡蛋、鱼肉、谷类、甘蓝菜、甜菜根、豆类、菠菜和西洋芹等获取。% [: A) j1 J$ n0 Z2 E
; c/ x) y) i. V x$ q4 k" f9 }" L
T细胞是人体淋巴细胞的主要组分,具有多种生物学功能,是身体中为抵御疾病感染、肿瘤形成的斗士。下图表示免疫细胞准备与入侵者战斗。 
* W0 {+ F `+ M; N% p) \7 S! H& D" m' {7 }0 ]8 U; _( Y# C/ t h
饿死肿瘤的药物
9 {# e4 {/ Q# S+ d5 \2 ]# Y- `6 s5 }2 m# a; \& u1 C4 n
6-重氮基-5-氧代-L-正亮氨酸(DON)是一种谷氨酰胺拮抗剂,最初是从秘鲁的土壤链霉菌中分离出来的。1956年Henry W Dion等人对这种非标准氨基酸重氮化合物进行了研究,认为作为谷氨酰胺的抑制剂可以用于抗癌。经过体外研究表明,DON处理可导致细胞凋亡,可以证明线粒体内膜被破坏,并观察到单链DNA断裂。确切的作用方式仍不清楚,需要进一步研究。
7 h1 [) L5 F6 }6 i k) b+ d' }
1 V% b: c% Y% a+ e/ w* j) D 1956年至1962年做了第一次临床研究,Magill及其同事评估了DON在63例患者中的单一作用。大多数患者患有不能手术的晚期实体瘤,包括肺、乳腺、结肠和泌尿生殖系统肿瘤,少数人患有白血病或淋巴瘤。结果是有效果。1980年至2000年进行了第二次五个I期临床研究。据报道,DON对人的肺、结肠和乳腺肿瘤有效。两个阶段的临床都有口腔粘膜炎、腹泻、恶心和呕吐的报道。DON的副作用太大,人们不得不再次停下来思考。
Y h$ O, g& z4 X8 ?$ I$ K
3 y% q+ k& J5 s, m3 x- Z' o# ] 1958年Adrien Albert在《自然》上发表文章提出在毒性很大的药物上“嫁接”一个氨基酸或其它的化学物质制成前体药物(简称前药),他用了prodrug这个词汇,后来他道歉说拼错了。前药没有生物活性或活性很低,在胃肠道无毒性,进入血液后被特定的酶切断变回原来的药物和氨基酸。
' U/ C+ ~& t" K8 y3 r- k3 e2 c- x- z+ P2 |+ x$ k6 `
2016年约翰霍普金斯大学等学者对DON嫁接,共制成22种DON前药。其中4a就是此次论文的化合物,如下图,其毒性小,抗癌效果好。这个化合物也叫JHU083 (Ethyl 2-(2-Amino-4-methylpentanamido)-6-Diazo-5-oxo-L-norleucine) (CAS:1998725-11-3)。 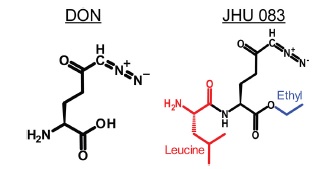
8 s% m$ e9 h: s/ t' o 除此之外约翰霍普金斯大学的学者还用JHU-083选择性阻断脑CD11b+细胞中的谷氨酰胺酶活性,并防止慢性社交挫败压力诱发的抑郁相关行为。# X7 a, b s4 w; I7 {1 o0 E
) I7 D- R/ g8 Y8 L
此外,还有一种叫CB839的另一种谷氨酰胺抑制剂现正在II期临床。
8 g: G& h+ q0 } O. t
7 b- g. j( J) {! l, a8 ^7 G JHU-083是饿死肿瘤最有希望的抗癌新化合物,盼JHU-083早日进入临床研究。
4 s; S; `- X' j6 Y3 S2 c/ }6 \+ g8 m3 D% b
|